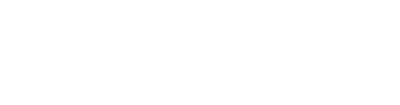Антидепрессанты могут негативно влиять на кишечник мужчин при длительном приеме
Ученые Медицинского института Новгородского государственного университета Павел Ховрин и Станислав Игнатьев исследовали влияние длительного приема антидепрессантов на микробиоту кишечника мужчин. Актуальность исследования обусловлена ростом числа случаев депрессии, особенно после пандемии COVID-19, которая, по данным Минздрава РФ, привела к психическим и неврологическим расстройствам у 99% переболевших.
О результатах исследования сообщил ТАСС один из авторов работы, Павел Ховрин. "Принято считать, что депрессия развивается под воздействием совокупности генетических факторов и экзогенного стресса. Однако микробиота кишечника играет ключевую роль в развитии депрессивных расстройств. Зарубежные исследования показывают, что некоторые антидепрессанты обладают противомикробным действием и могут подавлять жизнедеятельность микроорганизмов, включая выработку слизи и подвижность бактерий. На это влияет уровень серотонина и норадреналина в кишечнике, который может колебаться в зависимости от приема препаратов. Поскольку микробиом у людей сильно различается, это может объяснять, почему один и тот же препарат помогает не всем пациентам. Важно изучить, какой эффект оказывают эти препараты как в краткосрочной, так и в долгосрочной перспективе", — отметил Ховрин.
Исследование было сосредоточено на изучении воздействия популярного антидепрессанта "Сертралин канон" на микрофлору кишечника мужчин в возрасте от 18 до 40 лет, проходящих терапию от депрессивных расстройств. Препарат относится к классу селективных ингибиторов обратного захвата серотонина (СИОЗС), блокирующих каналы, транспортирующие серотонин.
Согласно результатам исследования, данный класс препаратов может оказывать двойственное влияние на микробиоту. При краткосрочном приеме наблюдается положительный эффект: увеличивается численность полезных бактерий, таких как Blautia, Coprococcus и Bifidobacterium, что сопровождается улучшением психоэмоционального состояния пациентов.
Однако при длительном применении препарата проявляется негативное воздействие. Исследователи установили, что подвижность бактерий и другие процессы их жизнедеятельности могут подавляться. Это стимулирует воспалительные реакции, гиперактивирует иммунную систему и усиливает выработку провоспалительных цитокинов. "При улучшении микробиоты психоэмоциональное состояние респондентов менялось в лучшую сторону. При длительном приеме наблюдались ухудшения: дисбактериоз, вздутие, диарея, частый метеоризм", — пояснил Ховрин.
Станислав Игнатьев добавил, что длительный прием селективных ингибиторов обратного захвата серотонина действительно оказывает двойное действие на микробиоту: сначала положительное, затем — нарушающее баланс микрофлоры. Врач, назначающий препарат, должен учитывать эти особенности и при необходимости снижать дозировку, чтобы избежать избытка серотонина, который может служить стимулятором воспалительных реакций.
Авторы подчеркивают, что выводы требуют подтверждения в масштабных клинических исследованиях для установления точной причинно-следственной связи. Тем не менее уже сейчас работа демонстрирует важность учета состояния кишечной микробиоты при назначении антидепрессантов и планировании долгосрочной терапии. Для получения более точных данных ученые планируют провести аналогичные исследования среди женщин.